1. Đại cương
Máy ghi biến cố tim vòng lặp cấy ghép được (Implantable Loop Recorder - ILR), còn được gọi là máy ghi biến cố tim là một thiết bị dưới da được sử dụng để chẩn đoán rối loạn nhịp tim. Các thiết bị này đã được cải tiến mạnh mẽ và thu nhỏ trong những năm qua cho thấy một số tính năng đáng tin cậy cùng với khả năng giám sát từ xa giúp cải thiện thời gian chẩn đoán và chiến lược theo dõi với khả năng giảm chi phí chăm sóc sức khỏe. Sự ra đời gần đây của ILR dạng tiêm làm cho thủ thuật này trở nên dễ dàng hơn và được người bệnh dung nạp nhiều hơn. ILR cho phép đánh giá tình trạng ngất tái phát không giải thích được với chẩn đoán không chắc chắn, cho thấy mối quan hệ có thể xảy ra với chứng rối loạn nhịp tim. Ngoài ra, gần đây nó đã được trang bị các thuật toán phức tạp có thể phát hiện các cơn rung tâm nhĩ. Cơ hội mới này có thể mang lại cho bác sĩ khả năng sàng lọc nhịp tim một cách có hệ thống với những tác động có thể có trong việc quản lý liệu pháp chống loạn nhịp và chống đông máu cho người bệnh. Việc sử dụng các thiết bị như vậy chắc chắn sẽ tăng lên vì chúng có thể hữu ích trong việc chẩn đoán một loạt các rối loạn và bệnh lý.
2. Chỉ định
Máy ghi biến cố tim được chỉ định trên người bệnh:
| Chỉ định | Diễn giải | Khuyến cáo | Mức độ chứng cứ |
|---|---|---|---|
| Đột quỵ không rõ nguyên nhân | Ở những người bệnh đột quỵ không rõ nguyên nhân, các thiết bị theo dõi điện tim bên ngoài không kết luận được, cấy máy theo dõi điện tim là hợp lý để tối ưu hoá khả năng phát hiện rung nhĩ thầm lặng | AHA/ACC/HRS 2019 | IIa |
| Ngất | Nếu đánh giá ban đầu không rõ ràng và nghi ngờ bệnh lý tim mạch | ACC/AHA/HRS 2017 | IIa |
| Hồi hộp | Có thể chỉ định trong trường hợp người bệnh có triệu chứng nặng, không thường xuyên và các máy theo dõi bên ngoài không ghi nhận | ESC 2009 | IIa |
| Rung nhĩ | Quản lý | Chưa có hướng dẫn |
3. Chống chỉ định
Người bệnh không đồng ý thực hiện.
4. Thận trọng
Có tình trạng rối loạn đông máu hoặc đang sử dụng kháng đông.
5. Chuẩn bị
5.1. Người thực hiện
- 03 bác sĩ.
- 03 điều dưỡng hoặc kỹ thuật y.
5.2. Thuốc
- Dung dịch sát khuẩn: povidone-iodine, cồn 70 độ.
5.3. Thiết bị y tế
- Hệ thống DSA.
- Thiết bị ghi biến cố tim vòng lặp cấy ghép được (ILR).
- Máy phân tích nhận cảm tạo nhịp.
- Điện tâm đồ 12 chuyển đạo cho thủ thuật.
- Máy sốc điện.
- Dụng cụ hồi sức: thuốc, nội khí quản, bóng ambu, mask, các loại dịch truyền.
- Máy tạo nhịp tim tạm thời và dây điện cực (khi cần thiết).
- Máy lập trình có thể đo được một số thông số cơ bản.
- Bơm tiêm và kim gây tê.
- Bộ dụng cụ tiểu phẫu vô khuẩn.
- Chỉ khâu.
- Bộ áo phẫu thuật, khăn mổ, gạc vô khuẩn, găng phẫu thuật.
5.4. Người bệnh
- Có chỉ định cấy máy ghi biến cố tim vòng lặp cấy ghép được (ILR).
- Người bệnh nhịn ăn 5 giờ trước khi được làm thủ thuật.
- Người bệnh được giải thích kỹ càng về mục đích tiến hành, cách thức tiến hành và các nguy cơ có thể gặp trong thủ thuật.
- Người bệnh hoặc gia đình viết giấy cam đoan làm thủ thuật.
- Dùng thuốc an thần nếu cần, nhất là khi thủ thuật kéo dài.
- Người bệnh được làm các xét nghiệm cơ bản: đông máu cơ bản, siêu âm tim, điện tâm đồ, chụp X-quang tim phổi,…
5.5. Hồ sơ bệnh án
- Bệnh án cần được hoàn thiện đầy đủ thủ tục hành chính, ghi nhận xét trong quá trình khám, điều trị và ghi y lệnh đầy đủ theo quy chế bệnh án.
5.6. Thời gian thực hiện kỹ thuật: 60 - 120 phút.
5.7. Địa điểm thực hiện kỹ thuật
- Phòng thực hiện kỹ thuật.
- Phòng phẫu thuật.
- Buồng bệnh.
5.8. Kiểm tra hồ sơ và người bệnh
- Đúng người bệnh (tên, tuổi, giới, căn cước, thẻ bảo hiểm và các giấy tờ theo quy định).
- Đúng chỉ định.
- Đúng loại thủ thuật dự kiến.
6. Tiến hành quy trình kỹ thuật
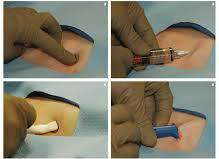
Hình 1: Quy trình thủ thuật
6.1. Bước 1: Người bệnh nằm ngửa.
6.2. Bước 2: Xác định đường dọc giữa xương ức, vị trí cấy máy nằm ở 3 khoảng liên sườn liên tiếp bên trái xương ức.
6.3. Bước 3: Gây tê bằng lidocain 2% 10 ml.
6.4. Bước 4: Rạch da.
6.5. Bước 5: Tạo đường hầm dưới da bằng dụng cụ chuyên biệt tương ứng với từng loại máy.
6.6. Bước 6: Cấy thiết bị ghi biến cố tim vòng lặp cấy ghép được vào đường hầm.
6.7. Bước 7: Kết nối với máy lập trình, kiểm tra tín hiệu nhận cảm, lập trình chức năng ghi nhớ và báo động của máy.
6.8. Bước 8: Khâu đóng vết thương theo lớp bằng chỉ vicryl 2/0 và nilon 2/0.
6.9. Kết thúc quy trình
- Đánh giá tình trạng người bệnh sau thực hiện kỹ thuật.
- Hoàn thiện ghi chép hồ sơ bệnh án, lưu hồ sơ.
- Bàn giao người bệnh cho bộ phận tiếp theo.
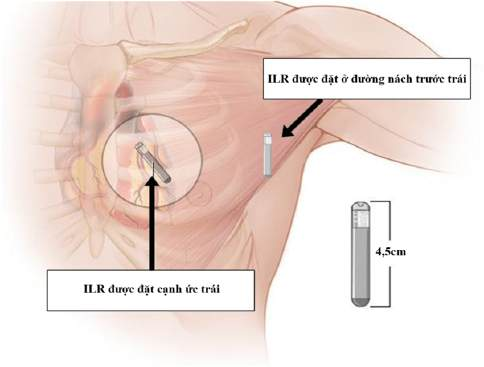
Hình 2. Các vị trí đặt ILR
7. Theo dõi và xử trí tai biến
- Theo dõi sát lâm sàng, sinh hiệu mạch, huyết áp, SpO2 trong quá trình thực hiện thủ thuật.
- Chảy máu: ép mạch tại vị trí chọc 5 - 10 phút, dùng các thuốc cầm máu nếu cần.
- Tràn khí màng phổi: chọc hút và dẫn lưu nếu tràn khí màng phổi nhiều.
- Tràn máu màng phổi: chọc hút và dẫn lưu.
- Phản ứng cường phế vị:
- Nâng cao 2 chân.
- Truyền dịch nhanh.
- Dùng atropin.
Tài liệu tham khảo
- January, C. T., Wann, L. S., Calkins, H., Chen, L. Y., Cigarroa, J. E., Cleveland Jr, J. C., ... & Yancy, C. W. (2019). 2019 AHA/ACC/HRS focused update of the 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society in collaboration with the Society of Thoracic Surgeons. Circulation, 140(2), e125-e151.
- Shen, W. K., Sheldon, R. S., Benditt, D. G., Cohen, M. I., Forman, D. E., Goldberger, Z. D., ... & Yancy, C. W. (2017). 2017 ACC/AHA/HRS guideline for the evaluation and management of patients with syncope: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Journal of the American College of Cardiology, 70(5), e39-e110.
- Task Force members; Brignole M, Vardas P, Hoffman E, Huikuri H, Moya A, Ricci R, Sulke N, Wieling W; EHRA Scientific Documents Committee; Auricchio A, Lip GY, Almendral J, Kirchhof P, Aliot E, Gasparini M, Braunschweig F; Document Reviewers; Lip GY, Almendral J, Kirchhof P, Botto GL; EHRA Scientific Documents Committee. Indications for the use of diagnostic implantable and external ECG loop recorders. Europace. 2009 May;11(5):671-87. doi: 10.1093/europace/eup097. Erratum in: Europace. 2009 Jun;11(6):836. PMID: 19401342.
- Kwok, Chun Shing, et al. “A review of the wide range of indications and uses of implantable loop recorders: a review of the literature.” Hearts 3.2 (2022): 45-53.
- Fasing, Kathleen, and Suzanne Benloucif. “ILRs-Implantable Loop Recorders, Insertion Guidance and After Care Precautions-A Review and Reflection of the Literature and Our Experience.” Biomedical Journal of Scientific & Technical Research 36.4 (2021): 28754-28760.
- Vilcant, Viliane, Omar Kousa, and Ofek Hai. “Implantable Loop Recorder.” StatPearls [Internet]. StatPearls Publishing, 2023.
- Đăng nhập để gửi ý kiến

